|
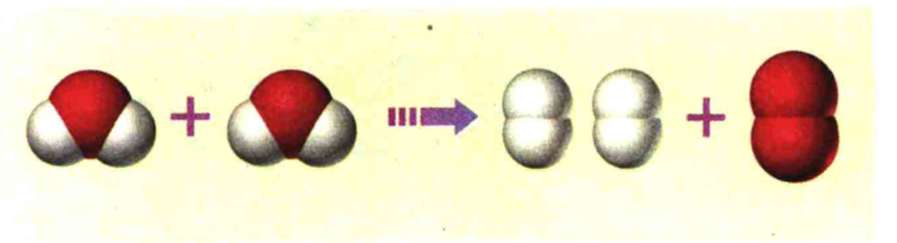
Мал. 15.5. Опис реакції розкладання води на молекулярному рівні
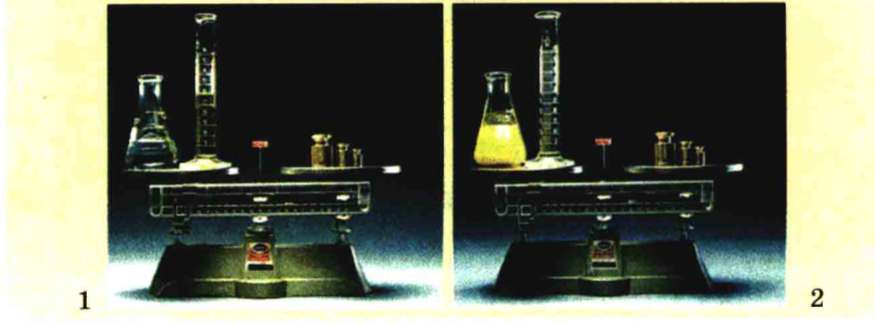
Закон збереження маси речовин. Оскільки атоми зберігаються, то має зберігатися і їхня маса. Для перевірки цієї гіпотези виконаємо дослід. Зрівноважимо терези, на одній шальці яких стоять посудини з розчинами натрій йодиду і плюмбум (ІІ) нітрату. Після змішування розчинів й утворення яскраво-жовтого осаду терези залишилися зрівноваженими. Отже, наша гіпотеза справдилася, і можна стверджувати, що маса реагентів дорівнює масі продуктів реакції (мал. 15.6).
Очевидно, що на основі одного досліду узагальнення робити не можна. Подібне дослідження реакції крейди з кислотою підштовхне нас до іншого висновку. Матимемо підстави стверджувати, що маса речовин зменшилася. Натомість маси продуктів прожарювання металів більші за маси металів, узятих для реакцій. Такого висновку ще у XVII ст. дійшов англійський науковець Роберт Бойль.
Яка ж з гіпотез правильна і як це довести? Як виявилось, достатньо змінити одну з умов експерименту. А саме - виконувати досліди в закритих посудинах.
Такий підхід дав змогу М.В. Ломоносову у звіті про свою наукову роботу за 1756 р. записати: «...роблено досліди в заплавлених міцно скляних посудинах, щоб дослідити, чи прибуває вага металів від чистого жару; оними дослідами знай-
|
|